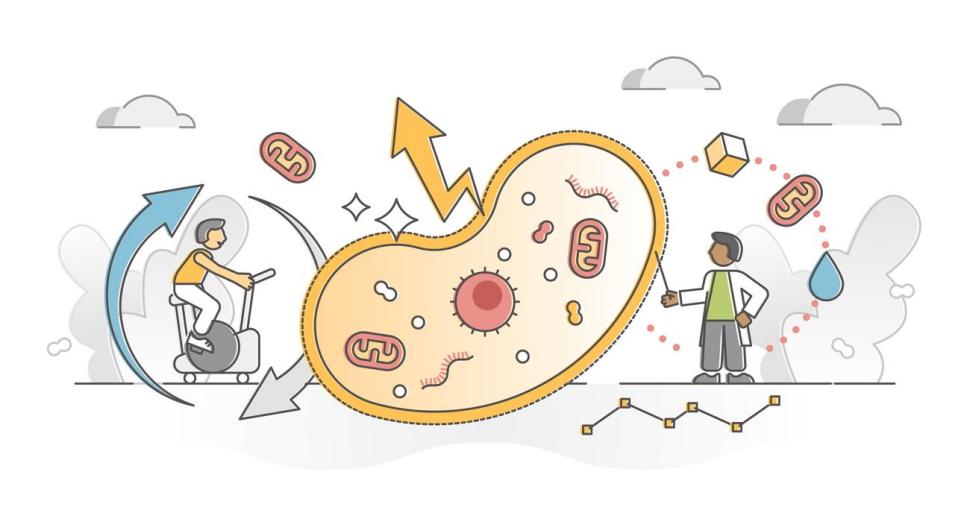
Dieta mitochondrialna skupia się na optymalizacji pracy mitochondriów – niezwykle ważnych, małych organelli komórkowych, które pełnią funkcję mikroskopijnych "elektrowni" w naszym ciele. Wspieranie ich funkcji prowadzi nie tylko do zwiększenia poziomu energii, ale również do poprawy funkcjonowania mózgu i prewencji wielu przewlekłych chorób metabolicznych.
Jak jedzenie zmienia się w energię?
Mitochondria są małymi, wewnątrzkomórkowymi organellami posiadającymi podwójną błonę: zewnętrzną oraz wewnętrzną, oddzielone przestrzenią międzybłonową. Ich głównym zadaniem jest produkcja energii w postaci adenozynotrifosforanu (ATP). Jest to uniwersalny nośnik energii, niezbędny do przeprowadzania większości funkcji życiowych organizmu1.
Proces, w którym nasze ciało przekształca zjedzony pokarm w energię, nazywa się oddychaniem komórkowym i zachodzi właśnie w mitochondriach. Z pożywienia, które spożywamy, organizm pozyskuje węglowodany, tłuszcze i białka.
W procesie trawienia są one rozkładane do prostszych cząsteczek, takich jak glukoza czy długołańcuchowe kwasy tłuszczowe, które następnie trafiają do komórek. Wewnątrz mitochondriów glukoza i kwasy tłuszczowe są utleniane w procesach takich jak beta-oksydacja oraz cykl kwasu cytrynowego (cykl Krebsa).
Z glukozy powstaje pirogronian, a jego przemiana w cyklu Krebsa jest kluczowa dla wytworzenia energii. Podczas tych reakcji z wiązań chemicznych w pokarmach uwalniane są elektrony o wysokiej energii, które są wychwytywane przez dinukleotyd nikotynoamidoadeninowy (NAD) oraz dinukleotyd flawinoadeninowy (FAD), redukując je do postaci NADH i FADH22. Te 2 cząsteczki przekazują następnie elektrony do tzw. łańcucha transportu elektronów, znajdującego się w wewnętrznej błonie mitochondrialnej.
Łańcuch ten składa się z 5 kompleksów białkowych. NADH oddaje elektrony do kompleksu I, natomiast FADH2 do kompleksu II. Obydwa kompleksy przekazują elektrony na koenzym Q (CoQ), który swobodnie dyfunduje przez wewnętrzną błonę mitochondrialną i dostarcza elektrony do kompleksu III, redukując cytochrom c. Następnie kompleks IV utlenia cytochrom c i przekazuje elektrony na tlen, w wyniku czego powstaje woda3.
Przepływ elektronów uwalnia energię, która jest wykorzystywana do pompowania protonów (przez kompleksy I, III i IV) z macierzy mitochondrialnej do przestrzeni międzybłonowej, tworząc gradient elektrochemiczny. Protony, dążąc do wyrównania stężeń, dyfundują z powrotem przez kompleks V (syntazę ATP), uwalniając energię niezbędną do syntezy ATP z ADP (adenozynodifosforanu). Proces ten nosi nazwę fosforylacji oksydacyjnej i dostarcza ponad 90% całkowitego ATP w komórkach4. Dlaczego mitochondria słabną?
Zrozumienie działania łańcucha oddechowego jest ważne, ponieważ to właśnie tam powstają reaktywne formy tlenu (ROS), potocznie nazywane wolnymi rodnikami. Gdy elektrony przepływają przez łańcuch, niewielka ich część "ucieka" i przedwcześnie reaguje z tlenem, tworząc rodniki ponadtlenkowe, a następnie nadtlenek wodoru. W reakcji Fentona nadtlenek wodoru może przekształcić się w wysoce szkodliwe rodniki hydroksylowe, które niszczą błony komórkowe, białka i DNA mitochondrialne (mtDNA)5.
Chociaż mitochondria mają potężny system obronny – m.in. enzym dysmutazę ponadtlenkową zależną od manganu, który znajduje się w macierzy – nadmiar kalorii, stres i toksyny mogą ten system przeciążyć6. Dochodzi wówczas do stresu oksydacyjnego, który prowadzi do degeneracji mitochondriów i rozwoju zespołu metabolicznego.
Co niezwykle ciekawe, mitochondria mają własne DNA (mtDNA) o strukturze kolistej. Ilość i funkcjonalność mitochondriów zależą właśnie od niego. Naukowcy odkryli, że zła dieta i otyłość mogą prowadzić do zmian epigenetycznych w mtDNA – w szczególności do jego metylacji (dodania grup metylowych CH3, które działają jak "flagi" regulujące odczyt genów) w obszarze zwanym D-loop.
Badania in vivo na populacji młodych dziewcząt wykazały, że u osób z nadwagą występuje zmniejszona liczba kopii mitochondrialnego DNA oraz podwyższony poziom jego metylacji w porównaniu do osób szczupłych. Oznacza to, że zła kompozycja ciała fizycznie osłabia nasze mitochondria7.
Czym jest zablokowany metabolizm?
Problemy z masą ciała, otyłość, zaburzenia lipidowe, zespół metaboliczny (MetS), a nawet cukrzyca typu 2, są w dużej mierze formą mitochondriopatii – czyli zaburzeń metabolicznych na poziomie mitochondriów. Głównym winowajcą jest tzw. zablokowany metabolizm pirogronianu.
Jak wspomniano wcześniej, glukoza z pożywienia powinna zostać przekształcona w pirogronian, który następnie zasila produkcję ATP. U osób z wtórną mitochondriopatią ten proces ulega blokadzie.
W sytuacji, gdy organizm nie może wykorzystać glukozy do wytworzenia energii (a my wciąż dostarczamy jej w nadmiarze w diecie), zostaje ona odłożona pod postacią tłuszczu zapasowego. Skutek jest podwójnie negatywny: po pierwsze tyjemy, a po drugie komórki produkują znacznie mniej mitochondrialnej energii ATP, przez co czujemy się nieustannie zmęczeni. Brak energii w komórkach sprawia, że narządy nie są w stanie spełniać swoich funkcji, co bezpośrednio prowadzi do poważnych chorób.
Jak odblokować metabolizm?
Aby odblokować metabolizm pirogronianu i usprawnić działanie naszych „minielektrowni” komórkowych, niezbędne jest zastosowanie zasad diety mitochondrialnej oraz modyfikacja proporcji makroskładników. Gdy przemiany glukozy zawodzą, organizm jako źródło energii może doskonale wykorzystywać tłuszcze. Oto szczegółowe, poparte nauką kroki odblokowujące metabolizm:
1. Zmiana proporcji makroskładników. Terapia zakłada, aby 50-60% dziennej podaży kalorii pochodziło ze zdrowych tłuszczów, 20-30% z białek, a jedynie 20-40% z węglowodanów złożonych.
2. Zdrowe źródła tłuszczów. Najlepiej wybierać właściwe rodzaje tłuszczów. Do spożycia na ciepło idealnie sprawdzą się masło klarowane, nierafinowany olej kokosowy oraz smalec. Na zimno warto stosować olej lniany, oliwę z oliwek, olej konopny czy olej z wiesiołka. Doskonałym źródłem tłuszczów są także awokado, jaja, wysokiej jakości mięso oraz małe ryby morskie (dziko żyjące) dostarczające kwasów omega-3.
3. Niski indeks glikemiczny (IG). Wysoki poziom insuliny i glukozy we krwi wyłącza procesy lipolizy (spalania tłuszczu) i ketogenezy. Najefektywniejsza dieta to ta, która opiera się na niskim IG. Węglowodany powinny pochodzić wyłącznie ze źródeł złożonych, takich jak pełnoziarniste zboża, kasze, brązowy ryż oraz warzywa.
4. Eliminacja węglowodanów prostych i produktów prozapalnych. Aby nie hamować metabolizmu, należy bezwzględnie odstawić rafinowany cukier, wyroby cukiernicze oraz białą mąkę. Szczególnie szkodliwa dla mitochondriów jest fruktoza (również ta ze słodkich owoców), która mocno obciąża wątrobę i wspiera stłuszczenie – należy więc wybierać owoce niskocukrowe, np. jagody. Dieta nakazuje również eliminację glutenu i nabiału (które u wielu osób nasilają stany zapalne) oraz alkoholu i kofeiny.
5. Koncepcja ciepłych śniadań. Opierając się na tradycyjnej medycynie chińskiej (TCM), śniadania powinno się spożywać na ciepło (np. owsianka z dobrym tłuszczem i żurawiną, jajecznica, kasze lub zupy). Dostarcza to energii narządom wewnętrznym, wzmacniając żołądek, śledzionę i nerki.
6. Równowaga kwasowo-zasadowa i nawodnienie. Zwiększona podaż tłuszczów i białek odzwierzęcych może przesuwać pH krwi w kierunku kwaśnym. Dlatego nieodłącznym elementem diety są warzywa wykazujące właściwości alkalizujące (odkwaszające) i woda – należy pić minimum 30 ml na każdy kilogram masy ciała. Dieta mitochondrialna zakłada zjadanie 5 porcji warzyw i owoców dziennie, z czego 80% powinny stanowić surowe warzywa.
7. Zdrowie jelit (mikrobiota). Prawidłowe wchłanianie mikroskładników jest niemożliwe bez zdrowych jelit, które są też miejscem syntezy witamin z grupy B i krótkołańcuchowych kwasów tłuszczowych. Należy spożywać błonnik oraz probiotyki pod postacią produktów sezonowych i fermentowanych (kiszonki: kapusta, ogórki).
8. Ostrożnie z dietą ketogeniczną. Chociaż taki sposób żywienia wspiera ketogenezę, należy unikać skrajnych reżimów ketogenicznych (węglowodany poniżej 10%), ponieważ ketogeneza pokrywa zapotrzebowanie mózgu na energię maksymalnie w 75%. Zbyt mała ilość węglowodanów grozi niedożywieniem tkanki nerwowej.
Okazuje się, że najlepszym globalnym modelem żywienia chroniącym mitochondria jest dieta śródziemnomorska, wykazująca silne właściwości antyoksydacyjne i przeciwzapalne.
Podczas gdy dieta zachodnia (obfitująca w smażone jedzenie, rafinowane węglowodany, czerwone mięso i cukry) indukuje dysfunkcje mitochondriów i spadek ich biogenezy, dieta śródziemnomorska obniża produkcję toksycznych rodników mtROS i podnosi aktywność oddechową komórek. Podstawą tej ochrony są mikroskładniki oraz związki bioaktywne pochodzenia roślinnego – polifenole i wielonienasycone kwasy tłuszczowe (PUFA). Badania in vitro i in vivo wykazały zbawienny wpływ konkretnych substancji naturalnych na strukturę i dynamikę mitochondriów:
Oliwa z oliwek (extra virgin)
Jest bogata w tyrozol i hydroksytyrozol (HT) zapobiega uszkodzeniom. W badaniach in vivo na modelu zespołu metabolicznego HT zmniejszał ilość białka Drp1 (odpowiedzialnego za patologiczne rozszczepianie mitochondriów) oraz normalizował ekspresję kompleksów I, II i V.
Ponadto u ryb z gatunku Megalobrama amblycephala hydroksytyrozol znacznie zwiększał zawartość ATP, liczbę mitochondriów oraz aktywność syntazy cytrynianowej poprzez pobudzenie szlaków PGC-1α i NRF1. Oliwa w połączeniu z azotanami zmniejsza również dysfunkcję śródbłonka9.
Kwasy tłuszczowe omega-3 (EPA i DHA)
Znajdujące się w rybach i owocach morza (oraz orzechach), kwasy te zwiększają ekspresję białek rozprzęgających (UCP3), redukując produkcję wolnych rodników. Skutecznie odwracają dysfunkcje mitochondrialnego łańcucha transportu elektronów i obniżają poziom zapalenia w organizmie10. Kwas chlorogenowy Zawarty w ziarnach kawy i jabłkach.
W eksperymentach in vitro wykazano, że chroni on komórki śródbłonka poprzez aktywację szlaku SIRT1 i kinazy AMPK, kluczowych dla biogenezy nowych mitochondriów11. Resweratrol Związek ten (obecny m.in. w ciemnych winogronach i jagodach) działa jak molekularny „trening” dla mitochondriów.
Poprzez de-acetylację i aktywację enzymu PGC-1α oraz sirtuin (SIRT1), bezpośrednio promuje powstawanie nowych organelli i zwiększa wydolność tlenową komórek. Badania kliniczne dowodzą, że u pacjentów z otyłością i cukrzycą typu 2 poprawia on funkcję mitochondrialną i utlenianie tłuszczów.12
Likopen
Ten karotenoid z pomidorów i grejpfrutów działa wysoce przeciwzapalnie. Zwiększa ekspresję genów odpowiedzialnych za budowę kompleksów łańcucha oddechowego (Cox5b, Cox7a1, Cycs) i zapobiega niebezpiecznej depolaryzacji błony mitochondrialnej13.
Kwas masłowy (maślan)
Powstaje w jelitach dzięki błonnikowi (obecny jest też w nabiale). W badaniach na myszach zwiększał utlenianie kwasów tłuszczowych poprzez podnoszenie poziomu CPT1b i enzymów cyklu Krebsa, a dodatkowo wzmagał ekspresję genów fuzyjnych (jak geny Mfn1, Mfn2 oraz Opa1), promując łączenie się mitochondriów w wydajne sieci, a blokując ich niszczenie poprzez geny Drp1 i Fis114.
Kwas ferulowy
Fenoskładnik znajdujący się w otrębach ryżowych. Usprawnia biogenezę i dynamikę mitochondriów, zwiększając ekspresję m.in. Pgc-1α, Nrf-1 oraz działając przeciwapoptycznie na białe krwinki15.
Apigenina i kwas elagowy
Apigenina występująca w owocach i warzywach chroni nerki i zapobiega atrofii mięśni poprzez hamowanie wycieku cytochromu c z uszkodzonych mitochondriów do cytozolu16. Natomiast kwas elagowy (z orzechów włoskich i truskawek) zapobiega zaburzeniom metabolicznym, oddziałując na mitochondria na 2 sposoby: bezpośrednio, zmniejszając ilość ROS i uszkodzenia mitochondriów lub pośrednio, przywracając całkowitą aktywność dehydrogenazy w mitochondriach poprzez utrzymanie kompleks II17.
Ekstrakt z kakao (flawanole)
Poprawia stosunek NAD+/NADH, stymulując zależne od nich enzymy (sirtuiny) do ochrony genomu mitochondrialnego i zwiększania masy tych organelli18.
Istotne suplementy
Sama dieta, mimo optymalizacji, może być w dzisiejszych czasach niewystarczająca z powodu postępującego ubóstwa gleb i ogromnej ilości stresorów. Terapia mitochondrialna mocno stawia na mitoceutyki – suplementy o ultrawysokiej czystości i przyswajalności (formy aktywne), zdolne przeniknąć przez błony komórkowe wprost do mitochondriów. Odpowiednia, celowana suplementacja w terapii mitochondrialnej obejmuje precyzyjne interwencje.
- Pierwszy etap. Aby odblokować metabolizm pirogronianu, niezbędne są aktywna postać witaminy B1 (benfotiamina) oraz kwas alfa-liponowy.
Substancje te są absolutnie krytyczne do przekształcenia pirogronianu w acetylo-CoA (związek wchodzący do cyklu Krebsa). Kwas alfa-liponowy to też potężny antyoksydant, doskonale wspierający ochronę narządów przed degeneracją i regenerujący mitochondria w wątrobie. Należy również pamiętać o makroelementach takich jak magnez (kofaktor ponad 300 reakcji enzymatycznych, wprost odpowiedzialny za produkcję ATP)19, cynk oraz potas.
- Etap drugi obejmuje zaawansowane wsparcie cyklu energetycznego. Konieczne jest wtedy włączenie aktywnych witamin z grupy B (B12, biotyny, kwasu foliowego, B2 i B3).
Witamina B2 jest fundamentalna do prawidłowej przemiany kwasów tłuszczowych na energię, natomiast B3 silnie modyfikuje i wspiera zachodzące procesy w łańcuchu oddechowym.
Kolejnym niezbędnym elementem jest koenzym Q10 – jeden z najważniejszych suplementów. Bez niego transport elektronów w błonie mitochondrialnej z kompleksu I i II do kompleksu III po prostu nie istnieje. Zwiększa drastycznie syntezę ATP i chroni jako wybitny przeciwutleniacz układ nerwowy, serce i wątrobę20.
W przypadku problemów z wątrobą zaleca się go stosować równolegle z manganem, który wspomaga własne mitochondrialne enzymy zwalczające wolne rodniki. L-karnityna w tym procesie działa jak „ciężarówka”, transportując długołańcuchowe kwasy tłuszczowe do wnętrza mitochondriów, by mogły one ulec beta-oksydacji i dostarczyć energii.
Bez niej, pomimo spożywania tłuszczu, komórki nie będą miały z niego pożytku Włączenie dinukleotydu NADH stymuluje i ułatwia pierwsze etapy fosforylacji oksydacyjnej. W walce z wewnątrzkomórkowym stresem oksydacyjnym sprawdzają się także silne interwencje wykorzystujące witaminy C i E.
Koenzym Q10 - niezbędny dla mitochondriów
Koenzym Q10 jest nie tylko niezbędny mitochondriom. Jak pokazuje obfita literatura, wspomaga on też leczenie licznych schorzeń układu krążenia, takich jak miażdżyca, kardiomiopatie (grupa chorób prowadzących do dysfunkcji mięśnia sercowego), arytmia, dusznica bolesna oraz nadciśnienie tętnicze. W randomizowanym, podwójnie zaślepionym, kontrolowanym badaniu przez rok porównywano wpływ doustnego leczenia koenzymem Q10 (120 mg/dzień) i witaminą B na czynniki ryzyka miażdżycy u pacjentów po ostrym zawale mięśnia sercowego.Po roku całkowita liczba zdarzeń sercowych, w tym zawał niezakończony zgonem i zgony sercowe były istotnie niższe w grupie interwencyjnej (otrzymującej Q10) w porównaniu z kontrolną. Naukowcy zauważyli, że u chorych poziom witaminy E w osoczu i cholesterolu HDL (lipoproteiny o dużej gęstości) wykazały istotny wzrost, podczas gdy substancje reagujące z kwasem tiobarbiturowym, malondialdehyd i koniugaty dienowe wykazały istotną redukcję w grupie CoQ w porównaniu do kontrolnej1.Jak wykazało 2-letnie badanie Q-SYMBIO, koenzym Q10 wyjątkowo dobrze sprawdza się w przypadku niewydolności serca, gdy mięsień nie daje rady prawidłowo pompować krwi.
W porównaniu do osób przyjmujących placebo ryzyko wystąpienia „poważnych działań niepożądanych w obrębie układu krążenia” u pacjentów z niewydolnością, którzy oprócz standardowych leków przyjmowali suplementy CoQ10, spadło o ponad 40%. Co więcej, o tyle samo obniżyło się ryzyko zgonu wywołanego chorobą serca i wszelkimi innymi schorzeniami2.
Ciekawym uzupełnieniem tych doniesień są wyniki badania interwencyjnego przeprowadzonego na Tajwanie. Uczeni dowiedli że suplementy koenzymu Q10 w dawce 150 mg mogą zmniejszać stres oksydacyjny i zwiększać aktywność enzymów antyoksydacyjnych u pacjentów z chorobą wieńcową. Oznacza to, że wyższa dawka suplementów koenzymu Q10 może sprzyjać szybkiemu i zrównoważonemu utlenianiu u tych chorych3.1. Mol Cell Biochem. 2003 Apr;246(1-2):75-82
2. Open Heart, 2015; 2: e000326
3. Nutrition. 2012 Mar;28(3):250-5
Zioła i roślinne ekstrakty botaniczne
Czerpiąc z mądrości fitoterapii i nowoczesnych badań farmakognostycznych, w diecie powinno znaleźć się miejsce dla imbiru (ekstrakty zawierające 6-gingerol podnoszą ekspresję białek szlaku AMPK i samego mtDNA)21.
Obiecujące wyniki daje też ekstrakt z zielonej herbaty (zawierający EGCG – galusan epigallokatechiny), który testowany klinicznie przyspieszał oksydację tłuszczów, oraz starożytny torf w połączeniu z ekstraktem z jabłek, co znacząco nasilało wytwarzanie ATP w mitochondriach u osób trenujących. Z kolei barwniki zwane delfinidynami, flawonoidy z kakao i kwas chlorogenowy pełnią funkcję łagodnych supresorów stanu zapalnego.
Przykładowy jadłospis
Teoria przekłada się na konkretne wybory na talerzu. W terapii tej kluczowe kluczowe są posiłki o stałych porach, unikanie przejadania się, dbanie o białko (ryby, strączki, drób, owoce morza) co najmniej w 3 posiłkach dziennie i wyparcie żywności wysoko przetworzonej (która zawiera zabójcze dla komórek kwasy tłuszczowe trans i konserwanty). Należy też bezwzględnie zastąpić oczyszczone zboża wariantami pełnoziarnistymi.
Oto jak może wyglądać optymalny dzień wspierający metabolizm tlenowy:
Śniadanie (na ciepło)
Omlet z warzywami przygotowany na maśle klarowanym. Jaja dostarczają pełnowartościowego białka i choliny (wspierającej funkcje mózgu), a warzywa (np. szpinak, pomidory) ogromu błonnika, witamin i przeciwutleniaczy. Taki posiłek daje zastrzyk energii bez wyrzutu glukozy.
Obiad
Pieczony łosoś posypany koperkiem i skropiony obficie oliwą z oliwek, podany z brokułami. Łosoś i oliwa dostarczają najcenniejszych lipidów wspierających płynność błon komórkowych (DHA, EPA, kwas oleinowy), a także wspierającą układ kostny witaminę D kolei brokuły to bogactwo związków siarkowych stymulujących detoks w wątrobie.
Kolacja
Można przygotować pieczonego, lekkiego kurczaka podanego z kaszą/ziemniakami, obfitą sałatą i pestkami. Kurczak dostarcza aminokwasów koniecznych do nocnej regeneracji. Jak wskazują zasady odblokowywania metabolizmu, węglowodany złożone spożywane wieczorem (jako mała przekąska) poprawiają jakość snu, umożliwiając prawidłową odnowę biologiczną.
- 1. Nutrients. 2022 Jul 28;14(15):3112
- 2. Chem. Rev. 2018;118:1460-1494
- 3. Curr. Opin. Struct. Biol. 2013;23:526-53; Nat. Rev. Mol. Cell Biol. 2015;16:375-38
- 4. BMC Biol. 2015;13:89; Int. J. Mol. Sci. 2021;22:5375
- 5. J. Mol. Biol. 2000;304:55-6; Circ. Res. 2014;114:524-537
- 6. Cell Biol. 2013;140:105-11
- 7. Front. Young Minds. 10:718698. doi: 10.3389/frym.2022.718698
- 8. Semin. Liver Dis. 2011;31:157-17; Am. J. Clin. Nutr. 2004;80:1-2
- 9. Free Radic. Biol. Med. 2014;67:396-407; J. Gerontol. A Biol. Sci. Med. Sci. 2020;75:2081-2088
- 10. Antioxid. Redox Signal. 2014;21:1156-1163
- 11. Mol. Nutr. Food Res. 2018;62:e1700928
- 12. PLoS ONE. 2015;10:e014429; Nature. 2006;444:337-342
- 13. Food Funct. 2019;10:2125-2137
- 14. Diabetes. 2017;66:1405-1418
- 15. J. Nutr. Biochem. 2017;48:51-61
- 16. J. Biochem. Mol. Toxicol. 2021;35:1-7
- 17. Hum. Exp. Toxicol. 2016;35:1060-1072
- 18. Diabetes Care. 2014;37((Suppl. S1)):S120-S143; Am. J. Clin. Nutr. 1995;61:1402S-1406S
- 19. Nutrients. 2013;5:3910-3919; J. Diabetes Res. 2016;2016:1260141
- 20. Methods Mol. Biol. 2021;2310:201-246; Int. J. Mol. Sci. 2021;22:770; Int. Rev. Cell Mol. Biol. 2018;340:209-344;
- 21. J. Food Sci. 2019;84:2101-2111

 Nasze magazyny
Nasze magazyny