Kluczem do zrozumienia procesów autoimmunizacji jest system odporności nabytej organizmu (swoistej). To trzeci etap ochrony przed drobnoustrojami - po naturalnych barierach i natychmiastowej reakcji odporności wrodzonej (nieswoistej) - nazywany również adaptacyjnym układem odporności1.
Oznacza on zdolność do rozpoznawania obcych antygenów, ich przetwarzania i przekazywania do wyspecjalizowanych komórek, które uruchamiają mechanizmy zwalczania określonego antygenu.
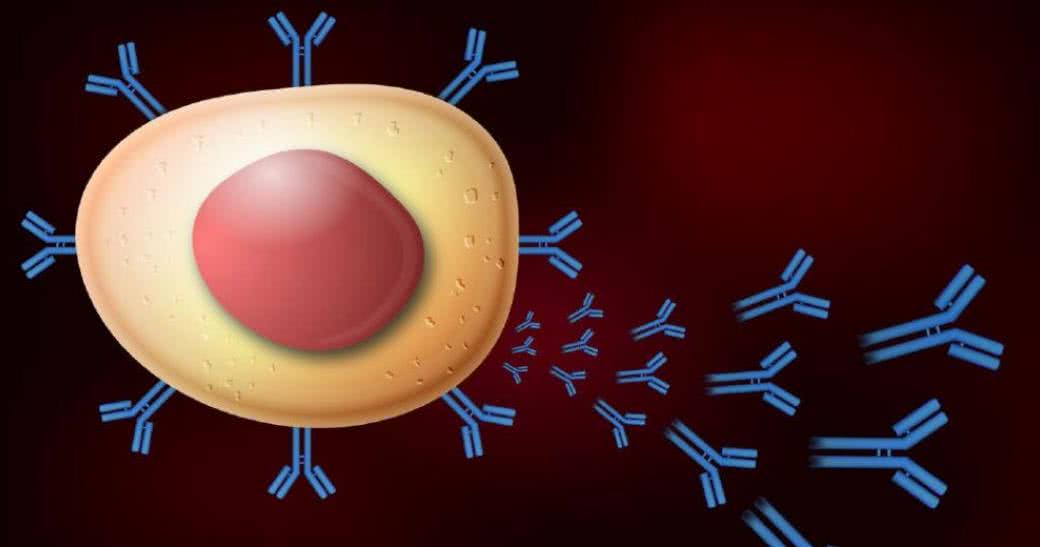
Odporność nabyta charakteryzuje się tzw. pamięcią immunologiczną, czyli zdolnością do szybkiego uruchomienia odpowiedzi immunologicznej na wcześniej poznany antygen. Innymi słowy organizm zapamiętuje infekcję, którą już przebył, a kiedy pojawia się ona ponownie, jest w stanie szybko na nią zareagować, ponieważ posiada już niezbędne do tego przeciwciała.
Komórkami odporności nabytej są limfocyty T i B, rozpoznające antygen przez swoiste receptory powierzchniowe (odpowiednio: TCR i BCR)2. Limfocyty T powstają głównie w grasicy, a B - w szpiku kostnym. Dzięki nim adaptacyjny układ odpornościowy ma praktycznie nieograniczoną zdolnością do odpowiedzi na każdą substancję - limfocyty B wytwarzają nawet ok. 1011 przeciwciał o różnej swoistości3!
Aby odpowiedź immunologiczna układu odporności nabytej przebiegła bez zarzutu, potrzebne są 2 elementy: identyfikacja antygenów zagrażających organizmowi oraz odróżnienie tych własnych od obcych. Nieprawidłowości na pierwszym etapie prowadzą do chorób alergicznych, w przebiegu których komórki układu odporności nabytej aktywują się w stosunku do antygenów obcych, ale niegroźnych (np. pyłków roślinnych).
Z kolei zaburzenie procesu rozróżniania własnych i obcych antygenów to właśnie przyczyna chorób autoimmunologicznych (autoimmunizacyjnych). Kiedy organizm rozpoznaje błędnie własne tkanki jako wroga, wytwarza i kieruje przeciwko nim przeciwciała. Dlatego mówimy o chorobach z autoagresji - nasz system odpornościowy atakuje bowiem własne komórki.
Swój czy nie, czyli siła kamuflażu
Choroby autoimmunologiczne są zatem efektem specyficznej, nieprawidłowej odpowiedzi immunologicznej, skierowanej przeciwko antygenom organizmu4. Przykładowo jeśli celem autoprzeciwciał są składniki otaczających nerwy osłonek, impulsy nerwowe przestają właściwie przewodzić informacje, a mięśnie zaczynają się kurczyć, w efekcie czego dochodzi do rozwoju stwardnienia rozsianego. Gdy zaś autoprzeciwciała błędnie skierują się przeciwko tkance jelit, występują choroba Leśniowskiego-Crohna i wrzodziejące zapalenie jelita grubego, a jeśli przeciwko tkance stawowej - reumatoidalne zapalenie stawów lub toczeń.
Łącznie znamy dziś ponad 70 jednostek chorobowych, które mają właśnie takie podłoże autoimmunologiczne. I chociaż każda z nich rozwija się nieco inaczej, można wyróżnić wspólne mechanizmy ich powstawania.
Według jednej z najstarszych teorii autoagresja jest efektem tzw. mimikry molekularnej, czyli upodabniania się patogenów do komórek organizmu5. Innymi słowy szkodliwe drobnoustroje, chcąc uniknąć zniszczenia, próbują przechytrzyć układ odporności i maskują się, aby przypominać prawidłowe struktury. Kamuflaż jest na tyle skuteczny, że limfocyty gubią się i atakują podobne komórki - zarówno obce, jak i własne.
Innym istotnym zjawiskiem jest przełamanie tolerancji immunologicznej wobec własnych antygenów. Aby zachować immunologiczną równowagę, autoreaktywne limfocyty - te, które potencjalnie mogą zaatakować własne tkanki - poddawane są eliminacji w procesie apoptozy. Dochodzi do tego w grasicy i szpiku kostnym, zanim trafią do tkanek obwodowych (tzw. tolerancja centralna)6. Natomiast te limfocyty autoreaktywne, które mimo wszystko przedostały się do obiegu, znajdują się w stanie uśpienia (anergii), tzn. nie otrzymują sygnału do aktywacji, dzięki czemu nie reagują na antygeny organizmu (tzw. tolerancja obwodowa).
Niestety mechanizmy tolerancji immunologicznej mogą zostać przerwane, co prowadzi do aktywacji autoreaktywnych limfocytów, np. pod wpływem infekcji7.
Toksyny i reszta
Chorobotwórcze baterie i wirusy, metale (takie jak rtęć i aluminium) czy silikonowe implanty piersi są związane z takimi schorzeniami jak toczeń rumieniowaty układowy i stwardnienie rozsiane.
Niektóre z tych toksyn, np. aluminium, kiedy są wykorzystywane w szczepionkach, nazywa się adiuwantami, ponieważ stymulują układ odpornościowy. Wiadomo, że mogą wywoływać kaskadę procesów immunologicznych, wstępnie objawiających się jako osłabienie, ból stawów i chroniczne zmęczenie. Przez lata te z pozoru nieszkodliwie stany stopniowo się nasilają, aż do manifestacji w postaci pełnoobjawowej choroby autoimmunologicznej32.
Dowiedziono, że inne "obce" składniki szczepionek powodują tzw. reakcję krzyżową, w przebiegu której komórki układu odpornościowego zwalczają elementy organizmu, tak jak postępowałyby w przypadku nieznanych patogenów, czyli niewłaściwie je identyfikują33. Poza wspomnianymi metalami jesteśmy również narażeni na pestycydy i zanieczyszczenia sieci Wi-Fi, chemikalia z farb, tworzyw syntetycznych, kosmetyków, używanych w domu środków czystości i detergentów i inne czynniki środowiskowe, które organizm musi nieustannie neutralizować.
Niektórzy ludzie radzą sobie z toksycznym obciążeniem bez większego problemu. Jednakże, w zależności od skłonności genetycznych, można być szczególnie wrażliwym na nieodłączne toksyny środowiskowe. Prawdopodobnie rosnąca liczba osób z chorobami autoimmunologicznymi to właśnie ta grupa najbardziej wrażliwa na bodźce środowiskowe. Dlatego należy dążyć do redukcji ekspozycji na toksyny oraz pobudzania naturalnego odtruwania organizmu. Przydatne mogą być regularne terapie oczyszczające, które pomogą pozbyć się złogów toksyn zalegających np. w jelitach.
Infekcje: dwie strony medalu
Udowodniono związek wielu chorób autoimmunologicznych z przebytym zakażeniem. Borelioza spowodowana jest ukąszeniem kleszcza zakażonego krętkiem Borrelia burgdorferi8. Niejasną patogenezę zespołu Guillaina-Barrégo (postępujący niedowład mięśni kończyn i oddechowych) wiąże się z przebytym szczepieniem przeciw grypie9 oraz zakażeniem Campylobacter pylori, które może wyzwalać ciąg zaburzeń prowadzących do autoimmunologicznego niszczenia struktur tkanki nerwowej w mechanizmie mimikry molekularnej10.
Podejrzewa się również związek między toczniem rumieniowatym układowym (choroba zapalna) i wirusem Epsteina-Barr (EBV)11 oraz stwardnieniem rozsianym (SM; zapalna, demielinizacyjna choroba ośrodkowego układu nerwowego) i infekcją Chlamydia pneumoniae12.
Największym potencjalnym szkodnikiem wydaje się jednak wirus zapalenia wątroby typu C (HCV), który może uczestniczyć w rozwoju cukrzycy typu 113, autoimmunologicznego zapalenia tarczycy, choroby Leśniowskiego-Crohna, zespołu antyfosfolipidowego oraz zapalenia naczyń (vasculitis)14.
Takich powiązań jest więcej, choć część z nich nie została jeszcze udowodniona.
Jednak wpływ infekcji na rozwój chorób autoimmunologicznych ma jeszcze drugie oblicze. Wydaje się, że w niektórych przypadkach mogą one wręcz chronić przed autoagresją. Zgodnie z teorią higieniczną coraz częstsze przypadki chorób autoimmunizacyjnych wiążą się z malejącą liczbą infekcji i poprawą warunków sanitarnych15. Przykładowo badania sugerują, że przebycie zakażenia Helicobacter pylori, CMV, EBV lub Toxoplasma gonidii może chronić przed cukrzycą typu 116.
Skąd ten protekcyjny wpływ? Prawdopodobnie, zgodnie z teorią współzawodnictwa, reakcja immunologiczna na infekcję ma pierwszeństwo przed autoagresją, ponieważ jest silniejsza17. Ponadto szczepienia, antybiotykoterapia czy stosowane środki odkażające niszczą całe populacje drobnoustrojów, które regulują funkcje odpornościowe i zapobiegają ich zaburzeniom (mikrobiom, czyli mikroskopijny ekosystem bakterii, wirusów i grzybów zasiedlających organizm ludzki od jelit po paznokcie stóp).
Paradoksalnie zatem rozwój higieny i medycyny, choć zmniejsza zapadalność na niektóre schorzenia, wpływa na rosnącą liczbę chorób z autoagresji.
Mozaika autoimmunizacji
Gdyby choroby z autoagresji wiązały się tylko z infekcjami, zapewne już dawno znaleźlibyśmy skuteczne metody ich profilaktyki i leczenia. Tymczasem sprawa jest bardziej złożona, ponieważ ta szeroka grupa schorzeń to wynik kombinacji wpływów genetycznych, immunologicznych, hormonalnych (czynniki endogenne) oraz środowiskowych (czynniki egzogenne). Obrazowo naukowcy nazwali to "mozaiką autoimmunizacji"18.
Przez lata najważniejszą rolę przypisywano tu czynnikom genetycznym, czyli mutacjom przekazywanym z pokolenia na pokolenie. Jednak chociaż udało się zidentyfikować liczne geny odpowiadające za autoagresję (związane głównie z tzw. układem zgodności tkankowej), coraz częściej mówi się o rosnącym znaczeniu czynników egzogennych, wśród których należy wymienić przede wszystkim wspomniane już infekcje, dietę, stres oraz narażenie na toksyny i inne zanieczyszczenia. Innymi słowy to współczesny tryb życia może w dużej mierze przyczyniać się do tego, że organizm traci orientację, który antygen jest "swój", a który wrogi.
Przykładowo ponad 80% pacjentów ze zdiagnozowaną chorobą autoimmunologiczną potwierdza, że wcześniej doświadczało podwyższonego poziomu stresu19. Prawdopodobnie wydzielane w stresujących sytuacjach hormony powodują rozregulowanie układu odpornościowego oraz produkcji cytokin zapalnych, a sam stres może być czynnikiem wyzwalającym rozwój choroby. Co więcej przewlekłe napięcie osłabia naturalne możliwości neutralizowania toksyn środowiskowych, które mają udowodniony wpływ na rozwój chorób z autoagresji (patrz ramka).
Podobnie udowodniono związek między paleniem tytoniu a reumatoidalnymi chorobami z autoagresji, takimi jak toczeń rumieniowaty układowy oraz reumatoidalne zapalenie stawów20. Nikotyna nie tylko jest tu czynnikiem ryzyka, ale również pogarsza przebieg już zdiagnozowanych chorób: u pacjentów odnotowuje się większe dolegliwości ze strony opłucnej i otrzewnej, a także częstsze bóle głowy i objawy neuropsychiatryczne. Nikotynizm wiąże się również z rozwojem stwardnienia rozsianego, choroby Gravesa-Basedowa czy pierwotnej marskości wątroby21.
Gdy zawodzi odporność wrodzona
Za odpowiedź zapalną organizmu odpowiadają 2 systemy odporności: nabytej, której zaburzenia leżą u podstaw chorób autoimmunizacyjnych, oraz wrodzonej. Ta druga jest ewolucyjnie starsza, a polega na uwarunkowanej genetycznie zdolności wykrywania białek lub polisacharydów typowych dla patogenów. Jej białka uczestniczą w rozpoznawaniu antygenów bakteryjnych i wirusowych oraz uruchamiają natychmiastową reakcję zapalną, eliminując zakażenie i ułatwiając procesy naprawcze.
Defekty genetyczne mogą jednak doprowadzić do sytuacji, w której elementy odporności wrodzonej generują nadmierną lub nieprawidłową reakcję zapalną. Taka nadreaktywność zapalna prowadzi do rozwoju tzw. chorób autoinflamatoryjnych34. Ponieważ procesy odporności wrodzonej i nabytej są powiązane, a zarówno choroby autoimmunizacyjne, jak i autoinflamatoryjne charakteryzują się stanem zapalnym, dostrzega się między nimi duży związek. Istotniejsze jest jednak to, co je różni.
W chorobach autoinflamatoryjnych istotną rolę odgrywają granulocyty obojętnochłonne i makrofagi (a nie limfocyty T i B), nie występują w nich autoprzeciwciała charakterystyczne dla autoagresji, a sam ich przebieg ma charakter okresowy (nie postępujący)35. Są one również uwarunkowane genetycznie - zwykle nieprawidłowość dotyczy jednego genu kodującego białka rozpoznające patogeny lub uruchamiające reakcję zapalną.
Do najczęstszych objawów chorób autoinflamatoryjnych należą: niereagująca na antybiotyki gorączka, zapalenia stawów, wysięki w błonach surowiczych, zapalenie otrzewnej, bóle mięśniowe, powiększenie węzłów chłonnych oraz zmiany skórne (np. wysypki)36. Z dość wąskiego spektrum chorób tego typu najlepiej poznana jest rodzinna gorączka śródziemnomorska (ang. familial mediterranean feler, FMF), wynikająca z mutacji genu MEFV kodującego białko purynę.
Trwającym od kilku godzin do 4 dni atakom gorączki towarzyszą silny ból brzucha i klatki piersiowej (spowodowane zazwyczaj zapaleniem otrzewnej), bóle stawów i niekiedy rumień kończyn dolnych37. Symptomy pojawiają się nieregularnie i ustępują samoistnie, ale brak leczenia objawowego może prowadzić do rozwoju amyloidozy (odkładania się złogów białek w narządach).
Antyzapalna dieta
Autoagresji może sprzyjać nawet nasza dieta. Produkty wysokoprzetworzone oraz niedobory witamin i minerałów osłabiają funkcjonowanie wszystkich komórek, w tym odpornościowych, już na poziomie mitochondriów. Organizm jest bardziej podatny na aktywność wolnych rodników i przestaje radzić sobie z usuwaniem na bieżąco toksycznych substancji. W efekcie traci zdolność reagowania na szkodliwe czynniki zewnętrzne i odróżniania ich od własnych antygenów, a kiedy już zachoruje - trudniej mu zahamować rozwój choroby.
Dlatego szczególnie istotna może okazać się dieta bogata w przeciwutleniacze, które zapobiegną szkodliwemu działaniu wolnych rodników i uchronią mitochondria przed nieodwracalnymi uszkodzeniami. Szczególną rolę odgrywają tu koenzym Q10 oraz witaminy C, D3 i z grupy B.
Przykładem może być niedobór witaminy D. W populacji kaukaskiej zaobserwowano, że zachorowalność na stwardnienie rozsiane jest wyższa w regionach o mniejszym nasłonecznieniu, a przebieg choroby (remisje i zaostrzenia) odpowiada sezonowym zmianom stężenia słonecznej witaminy w surowicy22. Wykazano również, że suplementacja zmniejsza ryzyko reumatoidalnego zapalenia stawów, a niedobór witaminy D u niemowląt (do 1. r.ż.) stanowi czynnik ryzyka zachorowania na cukrzycę typu 123. Co więcej jej pochodne stosowane są w leczeniu łuszczycy, po kilku tygodniach przynosząc poprawę nawet u 70-80% pacjentów24.
Z kolei zwiększenie spożycia wielonienasyconych kwasów tłuszczowych omega-3 może mieć korzystny wpływ na objawy tocznia rumieniowatego układowego, co wynika najprawdopodobniej z ich przeciwzapalnych właściwości25. Ponadto zwiększenie podaży kwasów omega-6, które powoduje wzrost proporcji między nimi a omega-3, może wiązać się z ryzykiem rozwoju choroby Leśniowskiego-Crohna, co zaobserwowano na przykładzie populacji japońskiej26. Zwiększenie podaży omega-3 stanowi również standardowe zalecenie w terapii reumatoidalnego zapalenia stawów (RZS)27. Udowodniono, że łagodzi ono poranną sztywność i ból stawów.
Co możemy zrobić?
Tak naprawdę już obserwacje dotyczące powiązania diety i zapadalności na choroby z autoagresji sprowadzają się do wniosku, że lepiej zapobiegać niż leczyć. I taką odpowiedź tak naprawdę daje dziś medycyna. Ponieważ nie zna ona dokładnych przyczyn i mechanizmów rozwoju tej grupy schorzeń, nie potrafi zagwarantować ich wyleczenia. Czasami oferuje jedynie spowalnianie ich przebiegu i odsuwanie w czasie nieuniknionej niepełnosprawności, jak przy stwardnieniu rozsianym.
W mniej zaawansowanych przypadkach sięga się po leczenie objawowe. W ruch idą zatem przede wszystkim farmaceutyki z grupy niesteroidowych leków przeciwzapalnych (NLPZ) i immunosupresyjnych (hamujących aktywność układu odpornościowego, np. kortykosteroidy). W jeszcze innych sytuacjach wdraża się terapię substytucyjną, których ten nie produkuje - tak jest w przypadku cukrzycy typu 1 (insulina) czy zapalenia gruczołu tarczowego typu Hashimoto (l-tyroksyna). Wciąż jednak jest to leczenie objawowe, a nie przyczynowe - a zatem łagodzące symptomy, ale nie likwidujące ich źródła. Co gorsza ma charakter długoterminowy, a w niektórych schorzeniach pacjent skazany jest na nie dożywotnio, co potęguje ryzyko skutków ubocznych.
W przypadku części chorób autoimmunologicznych (wrzodziejące zapalenie jelita, choroba Leśniowskiego-Crohna, reumatoidalne i łuszczycowe zapalenie stawów) skuteczna okazuje się neutralizacja cytokiny prozapalnej TNF za pomocą przeciwciał monoklonalnych28. Podejmuje się również próby leczenia za pomocą cytokin o silnych właściwościach przeciwzapalnych i immunosupresyjnych (IL-10 i IL-11). Póki co sprawdziły się one m.in. w reumatoidalnym zapaleniu stawów, ale odpowiedź na leczenie była jedynie tymczasowa29.
Inna z badanych ścieżek skupia się na próbach przywrócenia tolerancji immunologicznej na autoantygeny. Testuje się tu pochodzące z nich peptydy lub tzw. rekombinowane ligandy dla receptorów limfocytów T. Skuteczność tych ostatnich udało się na razie potwierdzić w eksperymentach na myszach30.
Duże nadzieje wiąże się również z tzw. zmienionymi ligandami peptydowymi (ang. altered peptide ligands, APL), czyli peptydami rozpoznawanymi przez autoreaktywne limfocyty T, które poddaje się nieznacznym zmianom (podmianie 1-2 aminokwasów w ich strukturze). Dzięki temu spada ich potencjał aktywujący limfocyty, a nawet może dojść do uśpienia limfocytu. Preparat zawierający APL znalazł już zastosowanie w leczeniu stwardnienia rozsianego31.
Póki co badania te to jedynie pojedyncze jaskółki, na których trudno opierać nadzieję na wyleczenie. Pozostaje jedynie walka z czynnikami ryzyka, czyli zrównoważona dieta, unikanie toksyn środowiskowych i stresu, detoksykacja czy wzmacnianie odporności. Być może brzmi to banalnie i mało przekonująco, ale nie należy lekceważyć siły codziennych nawyków. Historie 4 kobiet, które przedstawimy w kolejnym artykule z tego cyklu, są dowodem na to, że właśnie długotrwała zmiana najprostszych zwyczajów może odwrócić to, co lekarzom wydawało się nieodwracalne.
Bibliografia
- Nat Rev Immunol 2005; 5 (11): 866-879
- Trends Immunol. 2001; 22 (7): 356-360
- J Immunol 2005; 174: 1775-1781
- BMJ 2000; 321: 93-96
- Am Naturalist 1964; 321: 93-96
- J Immunol 1995; 154: 2588-2599
- Nature 1992; 359: 79-82
- Infect Immun 1995; 63: 2228-2235
- N Engl J Med. 1998; 339: 1797-1802
- Neurology 2007: 69: 1727-1728
- Ann N Y Acad Sci 2009; 1173: 658-663
- Ann Neurol 1999; 46: 6-14
- Autoimmune Rev 2008; 8: 18-23
- J Autoimmun 2009; 32: 261-266
- Br Med J 1989; 299: 1259-1260
- Ann N Y Acad Sci 2009; 1173: 633-639
- Cell 2004; 117: 265-277
- Isr Med Assoc J. 2008; 10: 8-12
- Rheum Dis Clin North Am 2000; 26: 4
- Nature Reviews Rheumatology 2007; 3: 707-715
- Lupus. 2006; 15 (11): 737-745
- Ann Neurol 2000; 47: 276-277
- Lancet 2001; 358: 1500-1503
- BMJ 2000; 320: 963-967
- Ann Nutr Metab 2009; 55 (1-3): 123-139
- Am J Clin Nutr 1996; 63: 741-745
- J Rheumatol 2000; 4: 115-121
- Expert Opin Biol Ther 2006; 6: 99-107
- J Rheumatol 2005; 32: 2102-2108
- J Immunol 2005; 175: 4103-4111
- Adv Neurol 2006; 98: 273-292
- J Autoimmun 2013; 47: 1-16
- Sci Transl Med. 2015; 7: 294ra105
- Best Pract Res Clin Rheumatol 2012; 26: 505-533
- J Immunol 2011; 187: 597-602
- Autoimmun Rev 2001; 12: 81-86
- Curr Med Chem. 2013; 21 (3): 261-269

 Nasze magazyny
Nasze magazyny