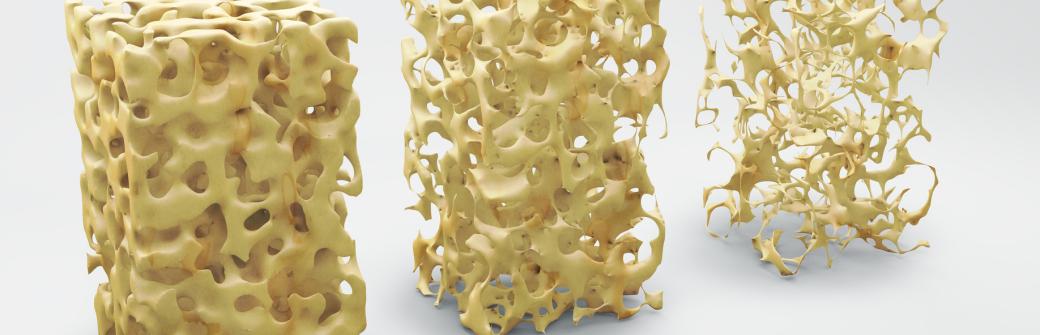
O osteoporozie mówi się zwykle w kontekście procesów starzenia, które mają największy związek z mechanizmami powodującymi stopniową utratę masy kostnej. Po pierwsze, spada ona po osiągnięciu szczytowej wartości ok. 30. r.ż. Po drugie, związane z menopauzą zmiany hormonalne (zwłaszcza spadek stężenia estrogenów) przyspieszają ten proces. To dlatego kobiety po 50. r.ż. należą do grupy zwiększonego ryzyka zachorowania (4 razy wyższego niż u mężczyzn).
Jednak problem osteoporozy jest o wiele bardziej złożony - zrzeszotnienie kości występuje w kilku postaciach, a do jego rozwoju mogą przyczyniać się różne czynniki (patrz ramka pt. "Choroba niejedno ma imię"). Tak naprawdę każde schorzenie przewlekłe, które trwa dłużej niż 6 tygodni, może sprzyjać rozwojowi osteoporozy wtórnej1. Lista potencjalnych winowajców jest naprawdę długa: znajdują się na niej niewydolność serca, niedoczynność i nadczynność tarczycy, cukrzyca, zaburzenia układu pokarmowego, jadłowstręt psychiczny i choroby zapalne stawów. W mniejszym stopniu metabolizm kostny pogarszają również zaburzenia czynnościowe nerek, nadczynność przytarczyc lub kory nadnerczy, przewlekła obturacyjna choroba płuc, białaczki i szpiczak2.
Choroba niejedno ma imię
Ze względu na etiologię wyróżnia się 2 podstawowe rodzaje osteoporozy: pierwotną (stanowi ok. 70% przypadków) i wtórną. Do pierwotnej zalicza się:
Osteoporoza idiopatyczna (młodzieńcza), związana z zaburzeniami wzrastania szkieletu w odniesieniu do norm wiekowych. Jej etiologia jest niejasna, ale podejrzewa się podłoże genetyczne lub endokrynologiczne, a także niedobór witaminy D, czynniki zakaźne i zaburzenia immunologiczne. Zwykle pojawia się przed okresem dojrzewania, a do jej objawów należą bóle w okolicy kręgosłupa i kończyn, osłabienie siły mięśniowej, wielomiejscowe złamania lub nieprawidłowy chód1. Część pacjentów zdrowieje samoistnie, ale u niektórych niezbędna okazuje się interwencja chirurgiczna.
Osteoporoza inwolucyjna, której istotą są zaburzenia metabolizmu kostnego. W typie I (pomenopauzalnym) utrata tkanki kostnej jest przede wszystkim wynikiem ustania funkcji endokrynnych gruczołów jajnikowych, czyli zmniejszenia stężenia estrogenów u kobiet po 50. r.ż. Z kolei typ II (osteoporoza starcza) dotyczy obu płci i pojawia się zwykle po 75. r.ż. w wyniku upośledzenia wchłaniania wapnia z przewodu pokarmowego, zmniejszenia poziomu witaminy D, pogorszenia funkcjonalności komórek kościotwórczych oraz ograniczenia aktywności fizycznej2.
Osteoporoza wtórna natomiast to choroba spowodowana konkretnymi czynnikami, innymi niż procesy starzenia. Do najczęstszych jej przyczyn należą zaburzenia hormonalne, ale może rozwinąć się również w wyniku niedoborów żywieniowych (zwłaszcza wapnia i witaminy D), nadużywania alkoholu (>2 porcji standardowych na dobę) oraz w przebiegu wielu chorób (od zaburzeń endokrynologicznych, przez cukrzycę i kłopoty z przewodem pokarmowym, po schorzenia układu krążenia i tkanki łącznej). Szczególny problem stanowi osteoporoza jatrogenna, będąca następstwem długotrwałego unieruchomienia lub stosowania niektórych leków, głównie glikokortykosteroidów, ale też tetracyklin, hormonów tarczycy, heparyny, środków przeciwdrgawkowych, moczopędnych, wywołujących hipogonadyzm (np. progesteron), uspokajających lub immunosupresyjnych3.
Bibliografia
- Przegl. Pediatr. 2006; 36 (2): 143-150; Calcif Tissue Int. 2002; 70: 395-397
- Prz Menoapuz 2010; 2: 113-117; Reumatol 2009; 47 (6): 360-363
- Post. Nauk Med. 2000; 13 (2): 31-37; Mayo Clin Proc 2006; 81 (5): 662-672; Med Prakt Reumatol 2011; 1: 3-40
1. Niewydolność serca prowadzi do osteoporozy
U pacjentów z chorobami układu krążenia często obserwuje się nieprawidłowości metabolizmu kostnego, których konsekwencją jest postępujący spadek masy kostnej skutkujący rozwojem osteoporozy. Obniżona masa kostna występuje nawet u 50% osób z niewydolnością serca, co znacznie przewyższa ten odsetek w ogólnej populacji3. Zwiększa to jednocześnie ryzyko złamań o różnej lokalizacji. W przeprowadzonej ostatnio analizie, która objęła 16 294 pacjentów, ustalono, iż prawdopodobieństwo złamań oraz związana z tym śmiertelność są u chorych z niewydolnością serca znacząco wyższe4.
Wydaje się, że zależności te wynikają z nieprawidłowości metabolizmu kości w przebiegu niewydolności serca. U pacjentów kardiologicznych dochodzi bowiem do zaburzeń gospodarki wapniowo-fosforanowej, przede wszystkim niedoboru wapnia i witaminy D3 oraz wtórnego wzrostu stężenia parathormonu (PTH), który uczestniczy w regulacji wchłaniania wapnia w przewodzie pokarmowym, jego wydalaniu przez nerki oraz odkładaniu i uwalnianiu z kośćca. Zwiększony poziom parathormonu kojarzony jest z nasileniem biochemicznych markerów resorpcji kości5. Z kolei przewlekłe stosowanie diuretyków przez pacjentów kardiologicznych przyczynia się u nich do zwiększonej utraty wapnia z moczem6.
Większość zgromadzonych dotąd danych wskazuje, iż niewydolność serca zwiększa prawdopodobieństwo osteoporozy. Nie ustalono dotąd, czy zależność ta działa również w drugą stronę, ale nie można zapominać, że liczne badania epidemiologiczne wskazują na związek między niską gęstością mineralną kości a miażdżycą w różnych lokalizacjach. A właśnie obecność depozytów wapniowych w naczyniach uznawana jest powszechnie za niezależny czynnik zwiększonego ryzyka sercowo-naczyniowego. Badania wskazują na istnienie zjawiska polegającego na zmniejszaniu się z wiekiem stopnia uwapnienia kości z równoczesnym zwiększeniem częstości występowania i rozległości zwapnień w dużych tętnicach oraz w obrębie zastawek, co nazywa się paradoksem kostno-naczyniowym7.
2. Kłopoty z tarczycą prowadzą do osteoporozy
Zarówno nadczynność, jak i niedoczynność tego gruczołu mają związek z większym ryzykiem zachorowania na osteoporozę. Wszystko przez to, że hormony tarczycy odgrywają istotną rolę w regulacji metabolizmu i przebudowy tkanki kostnej.
Hormony tarczycy wpływają pośrednio na aktywność osteoklastów i bezpośrednio na osteoblasty. Trijodotyronina (T3) tworzy z obecnymi w komórkach kościotwórczych receptorami jądrowymi kompleks aktywujący transkrypcję genu odpowiedzialnego za syntezę mRNA i białek macierzy kostnej oraz powoduje wzrost syntezy i wydzielania czynników wzrostu8. Nadmiar hormonów tarczycy przyspiesza zatem obrót kostny, powodując przewagę procesów resorpcji nad tworzeniem.
Tyroksyna skraca cykl przebudowy kości z 200 do 113 dni, powodując niedostateczne jej odtworzenie po resorpcji (w tym zmniejszenie grubości i zaburzenie struktury). Potwierdzają to badania, w których stwierdza się redukcję gęstości kości u kobiet z chorobą Gravesa-Basedowa w obrębie szyjki udowej (o 10%) i kręgosłupa (12%)9. Co więcej, ciężka nieleczona nadczynność tarczycy może prowadzić do przyspieszonego ubytku masy kostnej, łagodnej hiperkalcemii i wzrostu nerkowej utraty wapnia i obniżenia poziomu czynnego metabolitu witaminy D3. I chociaż w większości przypadków zmiany są odwracalne (przy skutecznym leczeniu nadczynności możliwy jest znaczący wzrost gęstości kości, choć nie zawsze osiągnie on wartości prawidłowe), biomechaniczne zmiany mogą powodować, że będą one mniej wytrzymałe na urazy, a tym samym - bardziej podatne na złamania10.
Z kolei niedoczynność tarczycy wiąże się z wyraźnym spowolnieniem procesów przebudowy tkanki kostnej. Obniżenie poziomu hormonów gruczołu powoduje bowiem spadek aktywności komórek kości. Tempo mineralizacji maleje wówczas nawet o 50%, a resorpcja nie przekracza 40% normy.
Jednak również w tym przypadku leczenie tyroksyną powoduje odnowienie tkanki kostnej, choć równocześnie prowadzi do czasowego wzrostu ryzyka złamań i obniżenia gęstości mineralnej (BMD), która dopiero po 2 latach od wdrożenia terapii wraca do normy11.
3. Cukrzyca prowadzi do osteoporozy
Insulina jest kolejnym hormonem istotnym dla macierzy kostnej. Dlatego w przypadku pacjentów z cukrzycą typu 1, u których całkowitemu zniszczeniu ulegają produkujące ją komórki beta wysp trzustkowych, gęstość mineralna kości jest zmniejszona od samego początku choroby12. Niedobór insuliny prowadzi m.in. do ograniczenia zdolności kościotworzenia przez osteoblasty.
Ostateczny mechanizm rozwoju osteoporozy w cukrzycy typu 1 wciąż pozostaje nieznany, choć na metabolizm kostny w tym przypadku mogą mieć wpływ zarówno insulinooporność, jak również czynniki wzrostowe i mediatory zapalne. Duże znaczenie przypisuje się także zmianom w zakresie wydzielania licznych hormonów powiązanych z metabolizmem kostnym, przede wszystkim estrogenów i androgenów. Późniejsze pokwitanie pacjentów z cukrzycą typu 1 często oznacza bowiem niemożność osiągnięcia szczytowej masy kostnej, wcześniejszą menopauzę oraz zaburzenia wydzielania hormonu luteinizującego (LH) i testosteronu u mężczyzn, co z kolei przyczynia się do wcześniejszego i zwiększonego ryzyka wystąpienia osteoporozy13. Inne istotne mechanizmy to zmniejszona resorpcja wapnia w jelicie, obniżenie poziomu witaminy D, krążącego parathormonu i magnezu. Jednak podstawowy wpływ na rozwój osteoporozy ma wyrównanie metaboliczne choroby, które sprzyja odbudowie masy kostnej14.
Wyniki norweskich badań Nord-Trondelag Health Survey wykazały również znamiennie większe ryzyko złamania szyjki kości udowej u kobiet z cukrzycą, przy czym podstawowe znaczenie miał dłuższy niż 5 lat okres trwania choroby. Dopiero po tym czasie masa kostna osiągała u nich znacznie niższe wartości. W innym badaniu prawdopodobieństwo przebycia złamania przez kobietę z cukrzycą typu 1 było nawet 25 razy większe niż w populacji ogólnej15.
Jeśli zaś chodzi o cukrzycę typu 2, w przeszłości panowało przekonanie, że u osób z tą chorobą osteoporoza i złamania osteoporotyczne występują rzadziej, co miało wynikać z prawidłowej masy kostnej. Dopiero badania przeprowadzone w latach 90. podważyły to domniemanie. Okazało się w nich, że osłabienie jakości tkanki kostnej może być również spowodowane przez charakterystyczne dla cukrzycy typu 2 zmiany w zakresie drobnych naczyń. Wykazano większą częstość złamań szyjki kości udowej, kości ramiennej i stopy u starszych kobiet z tą chorobą w porównaniu do grupy z prawidłową gospodarką węglowodanową. Wykazano także, że istotne znaczenie dla utrzymania odpowiedniej masy kostnej ma wyrównanie metaboliczne cukrzycy - jego brak powoduje nasilanie się osteoporozy, a przywrócenie w krótkim czasie prowadzi do zahamowania ubytku masy kostnej i stabilizacji mineralnej gęstości16.
Krzywica dorosłych czy zwyrodnienie stawów?
Osteomalacja to zespół chorobowy charakteryzujący się upośledzonym dojrzewaniem i mineralizacją nowo powstałej tkanki osteoidalnej w wyniku niedoboru witaminy D, wapnia bądź fosforu, występujący po zakończeniu wzrostu ciała. W konsekwencji dochodzi do gromadzenia się nadmiernej ilości osteoidu (miękkiej nieumineralizowanej tkanki kostnej) w miejscach jej przebudowy oraz zmniejszenia wytrzymałości kości. Odpowiednikiem osteomalacji u dzieci jest krzywica, cechująca się gromadzeniem tkanki chrzęstnej w częściach przynasadowych kości1.
Termin ten obejmuje całą grupę zaburzeń: od deficytów pokarmowych, upośledzenia wchłaniania i metabolizmu witaminy D, po defekty kanalików nerkowych. Ponieważ objawy kliniczne zwykle występują u ludzi starszych, często dochodzi do błędnego rozpoznania choroby zwyrodnieniowej stawów. Ponadto pacjenci z osteomalacją skarżą się na wiele symptomów związanych ze schorzeniami reumatycznymi, takich jak uogólnione bóle, męczliwość, miopatia, tkliwość okołostawowa i polineuropatia czuciowa2. Dominujące dolegliwości to uogólnione bóle kostne o charakterze stałym, dotyczące zwłaszcza miednicy, żeber i kręgosłupa, nasilające się podczas obciążenia kości, a także osłabienie proksymalnych mięśni kończyn dolnych, które może być przyczyną kołyszącego chodu.
W przypadku trudności diagnostycznych oprócz obrazowania rentgenowskiego i testów biochemicznych zaleca się badanie histomorfometryczne bioptatów kości (biopsja kośćca), które umożliwia bezbłędne rozpoznanie prawie wszystkich przypadków osteomalacji.
Bibliografia
- Nowa Medycyna - Osteoporoza 2004: 11, 3/2004 z. 125: 182-186; Nursing Older People 2014; 26 (6): 32-37
- Semin Arthritis Reum 1999, 28 (5): 287-304; Endocrine Journal 2015; 62 (8): 665-671
4. Zaburzenia pokarmowe prowadzą do osteoporozy
Również choroby układu pokarmowego, w szczególności przewlekłe, mogą przyczyniać się do rozwoju osteoporozy wtórnej. Dochodzi wówczas do zaburzenia wchłaniania wapnia, fosforu, magnezu oraz witamin D i K17.
Co więcej, u osób po gastrektomii (całkowita lub prawie całkowita resekcja żołądka) zaobserwowano zmniejszenie BMD od 10% do ponad 40%. Mechanizmy leżące u podstaw osteoporozy u tych chorych są niejasne.
Zrzeszotnienie występuje również u dzieci i młodzieży z jadłowstrętem psychicznym (anorexia nervosa), w szczególności u dziewcząt. W przypadku tej choroby w wyniku drastycznego odchudzania dochodzi do zaburzeń miesiączkowania, a następnie do utraty miesiączki. Niedobór estrogenów, nieodpowiednia podaż wapnia oraz wycieńczający wysiłek fizyczny powodują szybko postępujące odwapnienie szkieletu. Najnowsze badania dowodzą, że istnieje korelacja między czasem trwania braku miesiączki a gęstością mineralną kości, a ubytek masy kostnej może być nieodwracalny (zwłaszcza gdy brak miesiączki wystąpił przed 18. r.ż.)18.
5. Choroby nerek prowadzą do osteoporozy
Prawie u wszystkich pacjentów z przewlekłą niewydolnością nerek już we wczesnym okresie choroby dochodzi do osteodystrofii nerkowej, czyli zmian w obrębie kości, które mogą być wywołane przez zaburzenia metaboliczne i endokrynne (głównie zmieniony metabolizm parathormonu i witaminy D3 oraz upośledzenie czynności wydalniczych), a czasem bywają późnym efektem leczenia (np. przewlekłego stosowania preparatów glinu czy ograniczenia białka w diecie)19. Z kolei główną przyczyną hipokalcemii u chorych na przewlekłą niewydolność nerek jest upośledzenie wchłaniania wapnia z przewodu pokarmowego.
Osteoporoza jest coraz częściej stwierdzana również w następstwie coraz powszechniejszego leczenia nerkozastępczego u pacjentów w podeszłym wieku. Na jej występowanie wpływają mała aktywność fizyczna, niedobór estrogenów (u kobiet), częste stosowanie glikokortykosteroidów (np. przy kłębuszkowym zapaleniu nerek) oraz kwasica metaboliczna związana z długotrwałą chorobą (buforowanie zwiększonego ładunku jonów wodoru przez tkankę kostną powoduje utratę minerałów, której towarzyszy nasilenie resorpcji i zwolnienie kościotworzenia)20.
6. Zapalenie stawów prowadzi do osteoporozy
U pacjentów z przewlekłymi zapalnymi chorobami tkanki łącznej mogą występować zarówno inwolucyjne typy osteoporozy (pomenopauzalna i starcza), jak również wtórna. Często obserwuje się ją w przebiegu reumatoidalnego zapalenia stawów (RZS) - zwykle początkowo obejmuje nasady i przynasady kości tworzących staw zajęty procesem reumatoidalnym. Powstaje jako bezpośrednie następstwo reakcji zapalnej w jego obrębie. Zmiany występujące w błonie maziowej są zatem wynikiem przewlekłego, immunozależnego procesu zapalnego. W strukturze kostnej w okolicy zajętego stawu dochodzi do zwiększenia liczby osteoklastów oraz niszczenia okołostawowych struktur kostnych. W dalszym przebiegu RZS pojawia się osteoporoza uogólniona, najprawdopodobniej związana zarówno z rozwojem procesu zapalnego, stosowanym leczeniem, jak również z osłabieniem sprawności fizycznej - wszystkie te elementy nasilają resorpcję kości21.
Zmniejszenie masy kostnej obserwuje się również w zesztywniającym zapaleniu stawów kręgosłupa (ZZSK). Badania histologiczne wykazują u pacjentów defekt funkcji osteoblastów, polegający na nieprawidłowej mineralizacji tkanki kostnej już na początku choroby. Przyczyną tego stanu jest prawdopodobnie zaburzenie regulacji ich funkcji przez toczący się proces zapalny22. Duże znaczenie mają również leki stosowane w układowych chorobach tkanki łącznej, które co prawda mają działanie przeciwzapalne, ale jednocześnie wpływają na gospodarkę wapniowo-fosforanową oraz na osteoblasty i osteoklasty.
Artykuł ukazał się w numerze sierpień 2018 pt. "Kości w sieci powiązań".
Bibliografia
- Bromat Chem Toksykol 2008; 41 (4): 949-956
- Reumatol 2009; 47 (6): 360-363
- Am J Med. 1997; 103: 197-207; Clin Trnsplant 2010; 9999
- Circulation 2008; 118: 1946-1952
- Am J Med. 1997; 103: 197-207
- Circulation 2005; 111: 871-878; J Am Coll Cardiol 2005; 46: 142-146; J Bone Miner Metab 2003; 21: 247-252
- Eur Radiol 2008; 18: 2785-2807; Trends Mol Med 2009; 15: 405-416
- Endokrynologia Vol 5 no 8; 803-806; Przegl Lek 1998; 5 (55): 271-273
- J Clin Endocrinol Metab 1990; 70: 766; J Clin Encocrinol Metab 1991; 72: 1184-1188
- Thyroid 1994; 2 (4): 143-144; J Formos Med Assoc 1991; 90: 250-255; Thyroid 2002; 5 (12): 411-419
- Clin Endocrinol 1990; 33: 143-153
- Joint Bone Spine 2000; 67: 215-8; Bone 1993; 14: 29-33
- Hum. Reprod. 1999, 14: 298-302; J. Clin. Endocrinol. Metab; 1993, 76: 1048-53; J. Clin. Endocrinol. Metab. 1987; 65: 125-35; Diabetes 1996, 45: 1605-9
- Osteoporosis Int 2000, 11: 455-9
- Diabetologia 1999, 42: 920-25; Diabetes Care 2001; 24: 1192-7
- J. Bone. Miner. Res. 1997; 12:293-9; J. Clin. Endocrinol. Metab. 1997; 86: 32-38; Diabetes Res. Clin. Pract. 1994; 23: 43-54; J. Clin. Endocrinol. Metab. 1997; 82: 2915-20
- Endocr. Rev. 1995; 16: 87–116; Osteopor. Int. 1999; 2: S97-S110
- Endokryn Diabet. Chor. Przem. Mat. Wieku Rozoj 2003; 9(2): 67-71
- BMJ 1995; 310: 358; Am. J. Kidney Dis. 2001; 37: S54
- Am. J. Kidney Dis. 2004; 43: 566
- Bone 2002; 30: 340-346; Clin Exp Rheumatol 1995; 13 (Suppl 12): 21; J Clin Invest 2002; 110: 1419-27
- J Clin Invest 2005; 115: 1571-1579; Ann Rheum Dis 2010; 69: 592-7

 Nasze magazyny
Nasze magazyny